탁자이로 1150만원·이뮤도 1650만원 등재…발베사 10만1천원
엑스포비오 사용범위 확대로 36% 인하
위험분담계약제(RSA) 트랙을 밟은 고가 신약 5품목이 내달부터 보험적용을 받는다. 또한 급여가 확대된 신약은 가격을 확 낮춘다.

먼저, 탁자이로프리필드시린지주300mg는 성인 및 청소년(12세 이상)에서 유전성혈관부종발작의 일상적인 예방에 사용되는 신약으로, 현재 A7개국(미국, 영국, 독일, 프랑스, 이탈리아, 스위스, 일본)에 등재된 약제다.
심사평가원 급여적정성 심사를 위한 경제성평가 당시 RSA 대상에 해당돼 환급형으로 약가협상을 마치고 등재에 골인하게 됐다.
등재 약가는 1150만원이다.
이뮤도주는 진행성 또는 절제 불가능한 간세포암 성인 환자의 1차 치료로서 더발루맙과 병용요법에 효능효과를 인정받은 신약이다. 보험 선진국 중에선 미국, 영국, 독일, 프랑스 이탈리아, 스위스, 일본에 등재돼 있다.
업체 측은 2023년 6월 식약처 품목허가를 시작으로 업체 측은 이듬해인 2024년 6월 심평원 보험등재 결정신청을 했다.
2024년 5월 첫 결정신청 후 암질심에서 기준을 설정하자 자진취하 하고, 임핀지주가 담도암까지 급여기준을 확대 신청할 때 동시 검토를 요청해 11월이 돼서야 암질심을 통과할 수 있었다.
당시 약평위는 급여적정성이 있다는 판정과 함께 대체 약제의 RSA 내용 등을 고려해 약사협상 시 총액제한형 적용이 필요하며, 질환 특성에 따라 시장 점유율의 불확실성을 고려한 협상이 필요하다는 심의 결과를 냈다.
곧바로 이어진 협상명령에 따라 업체 측은 12월 건보공단과 약가협상과 예상청구액협상을 시작해 올 2월 초, RSA 환급형과 총액제한형 적용을 합의했다.
이뮤도주의 연간 대상 환자 수는 약 1700명 수준으로, 내달 등재 약가는 1650만원 수준이다.
발베사정은 이전에 최소 한 가지 이상의 PD-1 또는 PD-L1 억제제를 포함한 전신요법 치료 중 또는 치료 후에 질병이 진행된 FGFR3 유전자 변이가 있는 수술적으로 절제 불가능한 국소 진행성 또는 전이성 요로상피암 성인 환자 치료에 쓰이는 신약이다. 현재 미국, 영국, 독일, 프랑스, 스위스, 일본에 등재돼 있다.
심평원은 이듬해인 2025년 4월 말 암질환심의위원회(암질심)와 같은 해 8월 경제성평가소위원회(경평소위), 11월 약제급여평가위원회(약평위) 평가를 순차적으로 진행했다.
경평 결과, 당시 업체 측이 제시한 RSA 환급형을 반영한 비용-효용 분석 결과에 따른 비용효과비는 질병의 위중도, 사회적 질병부담, 혁신성 등을 고려한 기존 심의결과를 참고하면 수용 가능하다고 결론 냈다.
업체 측은 그 해 12월부터 이달 초까지 건보공단과 약가협상, 예상청구액 협상을 벌여 약가계약에 성공해 내달 급여 등재를 위한 준비를 마쳤다.
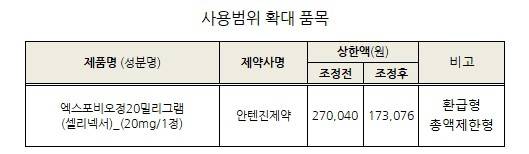
사용범위 확대 품목 = 적응증이 늘어나면서 사용범위가 확대돼 가격이 떨어지는 신약도 있다. 안텐진제약 엑스포비오정20mg인데, 이 약제는 이전에 한 가지 이상의 치료를 받은 다발골수종 성인 환자의 치료에 보르테조밉과 덱사메타손과의 병용요법으로 효능효과를 인정받았다. 보험 선진국 중에는 미국, 영국, 독일, 프랑스 이탈리아에 등재돼 있다.
이후 업체 측은 같은 해 10월 SVd 요법으로 식약처에 허가 변경을 신청했다.
11월에 급여기준 확대를 신청했고 심평원은 2025년 4월 말 암질심을 열어 평가를 진행했다. 복지부는 6월 비용효과성 분석 검토를 요청하고 같은 해 11월 약평위 심의를 통과했다.
당시 약평위에서는, 제약사가 가중평균가로 환산된 금액 이하를 수용할 경우 급여범위 확대의 적정성이 있다고 판정했다.
업체가 가격을 수용하고 곧바로 가격 협상에 들어갔다. 업체 측은 RSA 환급형과 총액제한형 트랙을 밟아 지난해 12월부터 이달 초까지 건보공단과 사용범위 확대 협상을 벌여 현재 보험약가에서 35.9% 떨어뜨린 17만3076원 수준으로 보험가격에 합의했다.