디앤디파마텍 "MASH 치료제 임상 2상 24주차서 유의미한 효과 확인"
조직생검 결과값과 연계된 F2-F3 단계 MASH 환자군에 대한 별도 하위그룹 분석 수행
디앤디파마텍이 대사이상 관련 지방간염(MASH) 파이프라인(신약후보물질) 'DD01'의 미국 임상 2상 시험의 24주 2차 평가지표 결과에서 유의미한 효과를 확인했다고 18일 밝혔다.
DD01은 디앤디파마텍이 자체 개발한 글루카곤 유사 펩타이드-1(GLP-1) 및 글루카곤 수용체를 동시에 타겟하는 장기 지속형 이중 작용제로, 현재 미국에서 대사이상 관련 지방간질환(MASLD)/MASH 환자를 대상으로 48주 투약 임상 2상 시험이 진행 중이다.
디앤디파마텍은 지난 6월 자기공명 양자밀도 지방비율(MRI-PDFF)로 측정한 12주차 결과에서 지방간이 30% 이상 감소한 환자 비율과 평균 지방간 감소율에서 모두 글로벌 경쟁사의 장기 투약(24-72주) 대비 경쟁력 있는 효과를 확인해 1차 평가지표를 달성했다.
회사는 24주 투약 이후 2차 평가지표인 섬유화 관련 혈액 바이오마커와 MASH 환자에서 높은 비중으로 동반되는 비만, 당뇨와 관련된 체중 및 혈당 결과를 분석했다. 또한 48주 투여 후 확인 예정인 조직생검과 연계해 임상적으로 주요한 환자군인 F2-F3 단계 섬유화를 동반한 MASH 환자에 대한 하위그룹 분석도 추가로 수행했다.
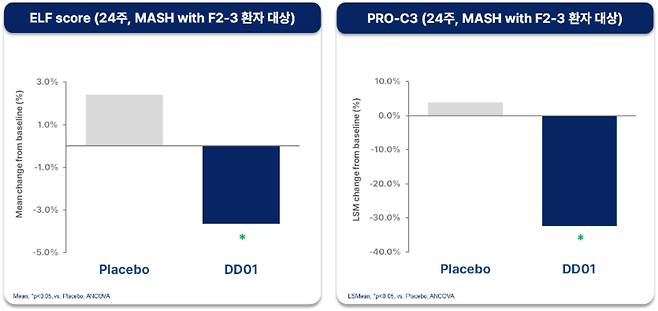
그 결과 12주차에서 의미 있는 개선을 보였던 섬유화 관련 바이오마커(ELF 스코어, PRO-C3)는 24주차에도 위약군 대비 지속적인 개선을 보여 DD01의 효과가 이어짐을 확인했다. 섬유화 진행여부를 비침습적으로 평가하는 ELF 스코어는 통계적으로 유의미한 차이를 달성했으며(p<0.02), PRO-C3도 통계적 유의성에 근접한 수준을 나타냈다(p=0.06). 특히 임상 및 허가 관점에서 중요한 치료 대상으로 간주되는 F2-F3 단계 섬유화를 동반한 MASH 환자군을 대상으로 한 하위 그룹 분석에선 ELF 스코어와 'PRO-C3' 모두 통계적으로 유의미한 개선이 확인되었다(p<0.05).
디앤디파마텍 관계자는 "핵심 타겟 환자군(F2-F3 동반 MASH)에서 확인된 섬유화 관련 바이오마커의 지속적 개선은 48주 투여 후 시행될 간 조직생검에서 긍정적인 결과가 도출될 가능성을 시사한다"며 "이번 24주차 분석에선 12주차에 확인했던 MRI-PDFF 및 MRE 등 영상 기반 평가는 최초 임상 설계에 포함되지 않아 수행되지 않았으며 추후 48주차에 추가로 진행될 예정"이라고 설명했다.
체중 관련 지표에서는 12주차에 전체 투약군 환자의 42.4%에서 체중이 5% 이상 감소한 반면, 24주차에는 그 비율이 51.5%로 증가했다. 또한 24주 투여 후 전체 투약군 환자의 평균 체중 감소율은 6.4%로 확인돼 MASH 치료제로서 경쟁력 있는 체중 감소 효과를 입증했다. 일반적으로 MASH 환자에선 GLP-1 계열 약물의 체중 감량 효과가 동반 질환이 없는 비만 환자 대비 30~40% 낮다는 점을 감안하면 DD01의 체중감소 효과는 MASH 치료제는 물론 비만 치료제로서도 경쟁력 있는 결과로 해석된다는 게 회사 측의 설명이다.
현재 진행 중인 DD01 임상 2상은 MASH에 최적화된 40mg 용량으로 진행되고 있다. 앞서 임상 1상 80mg 고용량군에서 안전성을 확보하면서 40mg 대비 높은 체중 감소가 나타난 것을 감안하면 향후 비만을 적응증으로 한 임상에선 80mg을 포함한 고용량 적용을 통해 더욱 우수한 체중감소 효과를 기대할 수 있을 것으로 전망된다.
DD01은 GLP-1과 글루카곤 비율을 최적화한 설계로 MASH 환자에게 흔히 동반되는 당뇨병 관리에도 긍정적 효과가 기대된다. 이번 24주 분석에서도 12주 결과와 동일하게 투여군은 위약군 대비 당화혈색소(HbA1c)가 통계적으로 유의하게 감소해 혈당 조절 효과가 지속된다는 것을 확인했다. 특히 당뇨병으로 진단되는 기저 당화혈색소 6.5% 이상의 환자군에서 24주 투여 후 당화혈색소 변화 결과(-1.08%)는 MASH 환자를 대상으로 한 세마글루타이드 2.4mg 72주 투여 임상 결과와 유사한 수준으로 나타났다.
최근 미국 식품의약국(FDA)에서 MASH 치료제 허가를 위한 비침습적 바이오마커인 순간탄성측정법(VCTE) 도입을 검토하기 시작하면서 향후 다양한 바이오마커가 치료제 허가 과정에 적극 활용될 것으로 보인다. DD01 임상 2상은 FDA가 검토 중인 초음파 기반 VCTE보다 정확성과 신뢰성이 높은 MRI기반 간 탄성도 측정법(MRE) 분석을 포함한다. MRE는 VCTE와 달리 간 전체를 포괄적으로 측정할 수 있어 보다 정밀한 섬유화 평가가 가능한 방법으로 인정받고 있다.
디앤디파마텍은 DD01 임상 2상의 12주 MRE 결과 전체 환자군에서 위약군 대비 통계적으로 유의한 개선이 확인됐으며, 이번에 추가로 수행한 12주차 하위그룹 분석의 F2-F3단계 섬유화 환자군에서도 동일하게 통계적 유의성을 확보한 효능을 입증했다고 설명했다.
DD01 임상 2상은 지난해 8월 첫 번째 환자의 48주 투약 완료를 시작으로 올해 연말까지 모든 환자의 48주 투약이 종료될 예정이다. 현재 모든 환자가 투약 종료 또는 30주 이상 투약을 진행 중이다. 이에 따라 FDA MASH 허가 요건에 필요한 간 조직생검 결과를 포함한 최종 주요 2차 평가지표 결과는 내년 상반기에 발표될 것으로 전망된다.
이슬기 디앤디파마텍 대표는 "이번 24주의 긍정적인 혈액 바이오마커 결과는 MASH의 미충족 수요인 간 섬유화 개선에 직접적 상관관계가 있는 뚜렷한 지방간 감소 효과에 기인한 DD01의 치료효과가 12주차 이후에도 지속되고 있음을 보여준다"며 "DD01이 MASH와 더불어 MASH 환자의 동반질환인 비만 및 당뇨를 동시에 치료할 수 있는 잠재력을 재차 보여준 결과로 해석된다"고 말했다. 이어 "회사는 이러한 긍정적인 임상 결과를 토대로 앞으로도 DD01 기술이전 계약 추진에 매진하여 성공적인 결과를 도출해 낼 수 있도록 최선을 다할 것"이라고 덧붙였다.
김선아 기자 seona@mt.co.kr
Copyright © 머니투데이 & mt.co.kr. 무단 전재 및 재배포, AI학습 이용 금지.
- "박명수 선 넘네" 주4.5일 비판→사연자 조언에 또 '시끌' - 머니투데이
- 서희원 동생 활동 복귀…'앙상한 모습' 구준엽은 여전히 묘소에 - 머니투데이
- '치과의사' 정희 "딸이 0순위…나는 출산 못 한다" 선전포고 - 머니투데이
- 장애 남편 '도우미'와 바람난 아내, 알고보니 전 남편이었다 - 머니투데이
- "강남 부럽다"…이상화 '브라톱 패션' 과감하게 드러낸 복근 - 머니투데이
- 삼성 노조, '영업이익 12%' 40조 성과급도 거절…이유 뭐길래 - 머니투데이
- "많이 먹었다"...'삼전닉스' 꽉 쥔 개미들, 이 종목은 팔았다 - 머니투데이
- "엄빠말 들을 걸"…'역대급 불장' 개미 수익률, 5060이 2030 이겼다 - 머니투데이
- "절대 안 팔아" 전원주 또 웃었다…코스피 불장 승리자 5060 투자법 - 머니투데이
- 벼랑끝 대한민국, '자멸의 길' 향하는 '삼성맨' - 머니투데이