美 FDA, 고위험군 대상 화이자 백신 부스터샷 승인
전체 맥락을 이해하기 위해서는 본문 보기를 권장합니다.
미국 식품의약국(FDA)가 고연령층 등 코로나19 고위험군에 대한 추가 접종(부스터샷)을 허용했다.
22일(현지시간) 로이터통신 등은 FDA가 △65세 이상 △18∼64세 중증 코로나19 고위험군 △18∼64세 면역 취약층 등 세 집단에게 화이자-바이오엔테크 백신의 1회분 추가접종을 하도록 긴급사용 승인(EUA)을 내렸다고 보도했다.
이 글자크기로 변경됩니다.
(예시) 가장 빠른 뉴스가 있고 다양한 정보, 쌍방향 소통이 숨쉬는 다음뉴스를 만나보세요. 다음뉴스는 국내외 주요이슈와 실시간 속보, 문화생활 및 다양한 분야의 뉴스를 입체적으로 전달하고 있습니다.
두 번째 접종 이후 최소 6개월 이후에 맞아야
모더나 추가 접종 여부도 검토..백신 격차 심해질 듯
[이데일리 김무연 기자] 미국 식품의약국(FDA)가 고연령층 등 코로나19 고위험군에 대한 추가 접종(부스터샷)을 허용했다. 앞서 화이자는 16세 이상을 대상으로 추가 접종을 허락해 줄 것을 요청했지만, FDA는 부작용 등의 이유로 고위험군에만 한정적으로 추가 접종을 허가했다.
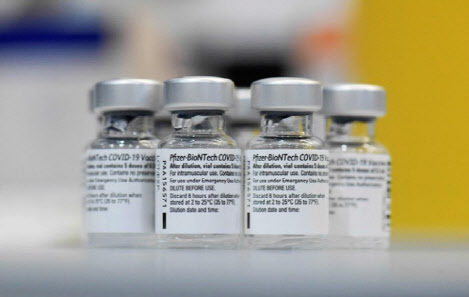
앞서 FDA 자문기구인 백신·생물의약품자문위원회는 지난 17일 회의를 열고 16세 이상을 상대로 면역 효과의 연장·강화를 위한 화이자 백신 추가 접종 승인 여부를 투표했다. 그 결과 반대 16표, 찬성 2표로 반대가 압도적으로 많아 해당 안건은 부결됐다. 당시 자문위원들은 기존의 2차 접종만으로 충분히 효과를 보고 있고, 3차 접종 시 젊은 남성들에게 심근염을 유발할 수 있다고 우려했다.
알버트 불라 화이자 최고경영자(CEO)는 FDA의 발표 이후 “추가 접종은 접종률을 높이기 위한 노력과 함께 이 질병의 지속적인 위협을 해결하는 데 중요한 역할을 한다고 믿는다”라면서 “FDA의 조치는 가장 취약한 사람들이 코로나19로부터 보호받을 수 있도록 돕는 중요한 단계”라고 평가햇다.
FDA의 이번 승인은 비록 화이자의 요구만큼 광범위하지 않지만, 향후 추가 접종의 안전성과 효능에 대한 더 많은 데이터를 수집할 수 있는 계기가 될 것이라고 블룸버그는 분석했다. 추가 접종 관련 데이터가 확보될수록 FDA가 추가 접종 대상자의 범위를 늘릴 수 있을 것이란 전망이다. FDA는 현재 모더나의 추가 접종 여부를 검토 중이다.
추가 접종의 효능에 대해선 여전히 갑론을박이 이어지고 있다. 뉴잉글랜드 의학저널에 실린 이스라엘 연구 논문에 따르면 화이자 백신의 추가 접종은 60세 이상 인구의 코로나19 관련 질병 발병률을 극적으로 낮출 수 있다. 반면, 일부 전문가들은 추가 접종에 쓸 백신을 1차 접종에 사용하는 것이 실효성이 더 크다는 반론을 제기하고 있다.
범위가 축소됐지만 미국에서 추가 접종이 허용됨에 따라 선진국과 빈곤국 간의 ‘백신 격차’를 지적하는 목소리가 높아질 것으로 전망된다. 테워드로스 아드하놈 거브러여수스 세계보건기구(WHO) 사무총장 등은 선진국 일부가 백신을 독점해 추가 접종에 나서는 것이 코로나19 세계적 대유행(팬데믹)을 종식하는데 걸림돌이 될 것이라고 비판한 바 있다.
김무연 (nosmoke@edaily.co.kr)
Copyright © 이데일리. 무단전재 및 재배포 금지.
- [단독]"연봉 천만원 인상·자사주 달라"..삼성전자 노조 요구안 '논란'
- 김범수 개인회사 자녀들 퇴사…"인재양성으로 사업목적도 바꿀 것"
- "월 500만원 벌고 집 있는 남자"…39세女 요구에 커플매니저 '분노'
- "안전벨트 안 맸네?"…오픈카 굉음 후 여친 튕겨나갔다
- 개그맨 김종국 子, 사기 혐의 피소…"집 나가 의절한 상태"
- [단독]SK 이어 롯데도 중고차 `노크`…대기업 진출 현실화 임박
- "겸허히 받아들여"…프로포폴 실형 면한 하정우, 향후 행보는 [종합]
- '돈나무 언니' 캐시 우드 “비트코인·테슬라로 막대한 수익 얻을 것"
- '尹 장모 대응문건' 의혹에 추미애 "대검이 장모 변호인 역할 한 셈"
- 文대통령, 퇴임 후 '캐스퍼' 탄다.. ‘광주형 일자리 SUV’ 예약