셀트리온 램시마SC, 캐나다 판매 허가 획득
전체 맥락을 이해하기 위해서는 본문 보기를 권장합니다.
셀트리온(068270)이 인플릭시맙 피하주사 제형 자가면역질환 치료제 '램시마SC'의 판매 허가를 획득한 것으로 확인됐다.
31일 관련 업계에 따르면 캐나다 보건청(Health Canada)은 지난 28일 셀트리온의 램시마SC에 대한 판매 허가를 승인했다.
셀트리온 관계자는 "28일 캐나다 보건청이 램시마SC에 대한 판매 허가를 승인한 것으로 확인했다"고 말했다.
이 글자크기로 변경됩니다.
(예시) 가장 빠른 뉴스가 있고 다양한 정보, 쌍방향 소통이 숨쉬는 다음뉴스를 만나보세요. 다음뉴스는 국내외 주요이슈와 실시간 속보, 문화생활 및 다양한 분야의 뉴스를 입체적으로 전달하고 있습니다.
캐나다 자가면역질환 치료제 시장 약 2조원
미국 FDA에서도 임상 3상 진행 중
[이데일리 왕해나 기자] 셀트리온(068270)이 인플릭시맙 피하주사 제형 자가면역질환 치료제 ‘램시마SC’의 판매 허가를 획득한 것으로 확인됐다. 2019년 유럽의약품청(EMA)으로부터 판매 승인을 획득해 출시국가를 늘리고 있는데다 북미 지역에서도 판매 허가를 받으면서 관련 매출이 확대될 것으로 보인다.
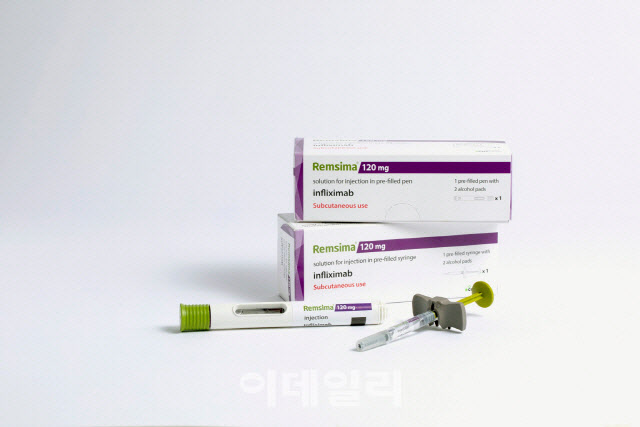
램시마SC는 셀트리온이 개발한 자가면역질환 치료용 바이오시밀러 램시마(성분명 인플릭시맙)를 정맥주사(IV) 제형에서 피하주사(SC) 제형으로 바꾼 제품이다. 정맥 속에 바늘을 찔러 약물을 주입하는 제형에서 피부 아래 조직에 소량을 투약하는 제형으로 변경한 것이다. 투약 시간이 짧고 병원에 갈 필요 없이 환자가 직접 투여할 수 있는 장점이 있다.
이번 판매 허가는 셀트리온이 지난해 2월 램시마SC에 대한 허가를 신청한 지 1년 만에 나온 결과다. 캐나다 보건청은 EMA에 셀트리온이 제출한 방대한 임상 데이터를 인정해 ‘바이오베터(Biobetter)’ 형태로 허가 심사를 진행했다. 제약업계는 캐나다가 의료 재정 절감을 위해 바이오시밀러에 대해 우호적인 정책을 펴고 있어 이번 허가가 조속히 이뤄졌고 이후 시장 진입도 순조로울 것으로 보고 있다. 셀트리온은 자회사인 셀트리온헬스케어를 통해 현지에 의약품을 판매할 예정이다. 회사가 추산하는 캐나다 자가면역질환 치료제 시장 규모는 2조원이다.
캐나다를 시작으로 북미 지역 전체에서 판매 허가를 받게 되면 잠재적인 시장 규모는 더욱 커질 전망이다. 북미 지역의 자가면역질환 치료제 티엔에프알파(TNF-α) 억제제 시장은 42조원 규모로 추산된다. 미국 식품의약국(FDA)에서는 램시마SC를 ‘신약’으로 판단, 셀트리온은 FDA와의 협의 하에 1·2상 임상을 면제받고 2019년 7월부터 임상 3상을 진행 중이다.
앞서 셀트리온은 2019년 EMA로부터 판매 승인을 받고 독일, 영국 프랑스 등 주요 5개 국가 출시를 진행하고 있다. 지난해에는 류마티스 관절염(RA)에 이어 염증성 장질환(IBD)에 대한 추가 적응증 승인을 받기도 했다.
왕해나 (haena07@edaily.co.kr)
Copyright © 이데일리. 무단전재 및 재배포 금지.
- 셀트리온 “렉키로나주 임상 3상 이미 착수…환자 모집 속도 빨라”
- "설, 거주지 다르면 집에서 만나도 5인 이상 가족 모임 불가능"(종합)
- 강다니엘, 서울가요대상 본상 "비장한 마음으로 새해 준비"
- "더 이상 못 참아"…거리두기 연장에 소상공인 '분노'
- [국회기자24시]‘파란 운동화’ 신고 뛰는 박영선, 3년 만에 꺼낸 이유는
- [전문] 진달래 "학폭 인정, 미스트롯2 하차 예정"
- 금태섭 "안철수, 서울시장 제3지대 경선하자"
- 948회 로또 1등 11명 21억씩…7명 수동 선택
- [이주의1분] 모델 최소라의 '떡볶이 먹방', 진짜 '난리났네 난리났어'
- 이낙연 "김종인, `이적 행위` 본인 발언 책임있게 정리해야"