"셀트리온 코로나 치료제, 시판 후 3상 결과 제출 조건부 허가 권고"
전체 맥락을 이해하기 위해서는 본문 보기를 권장합니다.
식품의약품안전처의 법정 자문기구인 중앙약사심의위원회가 셀트리온의 코로나19 항체치료제 '렉키로나주'에 대해 시판 후 임상 3상 시험 결과 제출을 전제로 품목 허가가 가능하다는 의견을 내놨다.
식약처는 "중앙약심은 렉키로나주의 품목허가 신청을 위해 제출한 자료에 따른 안전성과 효과성을 검토한 결과와 국내 코로나 대유행 상황, 코로나19 치료제에 대한 환자 접근성과 의료진의 선택권 등을 종합적으로 고려했을 때, 신청 품목의 국내 환자에 대한 필요성이 인정돼 3상 임상시험 결과를 제출하는 것을 조건으로 품목허가 할 수 있을 것이라고 자문했다"고 밝혔다.
이 글자크기로 변경됩니다.
(예시) 가장 빠른 뉴스가 있고 다양한 정보, 쌍방향 소통이 숨쉬는 다음뉴스를 만나보세요. 다음뉴스는 국내외 주요이슈와 실시간 속보, 문화생활 및 다양한 분야의 뉴스를 입체적으로 전달하고 있습니다.
(지디넷코리아=김민선 기자)식품의약품안전처의 법정 자문기구인 중앙약사심의위원회가 셀트리온의 코로나19 항체치료제 '렉키로나주'에 대해 시판 후 임상 3상 시험 결과 제출을 전제로 품목 허가가 가능하다는 의견을 내놨다.
또한 경증환자에 대해서는 임상시험에서 유의미 한 결과를 확인하지 못했기 때문에 제한된 환자군에만 투약할 것을 권고했다.
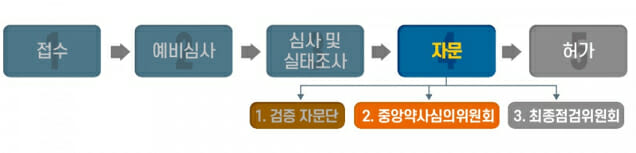
식약처는 27일 충북 오송 식약처 본부에서 개최한 중앙약사심의원회(이하 중앙약심) 회의 결과를 발표했다. 식약처는 세 단계 전문가 자문 절차 가운데 두 번째인 중앙약심에 셀트리온 렉키로나주의 안전성과 효과 등에 대해 중앙약심에 자문했다.

통상 품목 허가를 받으려면 임상 3상까지 진행해야 하지만 코로나19 대유행이 지속되는 가운데, 중앙약심은 렉키로나주가 시판 뒤 3상 시험결과를 제출하는 것을 전제로 조건부 품목허가를 낼 수 있다고 판단했다.
식약처는 "중앙약심은 렉키로나주의 품목허가 신청을 위해 제출한 자료에 따른 안전성과 효과성을 검토한 결과와 국내 코로나 대유행 상황, 코로나19 치료제에 대한 환자 접근성과 의료진의 선택권 등을 종합적으로 고려했을 때, 신청 품목의 국내 환자에 대한 필요성이 인정돼 3상 임상시험 결과를 제출하는 것을 조건으로 품목허가 할 수 있을 것이라고 자문했다"고 밝혔다.
다만 경증 환자에 대한 임상시험에 대한 유의미 한 결과는 충분하지 못해, 중등증 환자와 고위험군 경증 환자를 대상으로 렉키로나주를 투약할 것을 권고했다.
일부 위원들의 경우 소수의견으로 의약품 품목 허가보다는 특례 제조 승인 등을 활용하는 안에 대해 제안했다.
식약처는 이번 중앙약심 권고사항 등을 종합한 뒤 최종점검위원회를 통해 렉키로나주의 허가 여부를 최종 결정할 예정이다.
식약처는 코로나19 대유행 상황을 감안해 코로나19 백신/치료제 안전성·효과성 검증 자문단과 최종점검위원회를 추가로 구성해 3중의 자문 절차를 거친다.
김민선 기자(yoyoma@zdnet.co.kr)
Copyright © 지디넷코리아. 무단전재 및 재배포 금지.
- 셀트리온, 청주공장 사전충전형 주사기 생산라인 준공
- 셀트리온, '프롤리아' 바이오시밀러 임상 3상 본격화
- 셀트리온 "코로나19 치료제, 중증 발생률 54% 줄여"
- 셀트리온, 인천 송도 바이오클러스터 구축 지원 프로젝트 가동
- 셀트리온, 코로나19 항체치료제 글로벌 임상 2상 완료
- 美, 삼성 반도체 보조금 6.9조원 확정…원안 대비 26% 줄어
- "그래도 가야돼" CES 향하는 中 기업들…비자 문제는 변수
- 美 체류 늘린 정용진, 트럼프 깜짝 만남 여부 관심↑
- [AI는 지금] 규제 갈림길 선 AI, 진화 속도 빨라졌다
- [1분건강] 폐암 환자 10명 중 4명은 비흡연자